الفيديوات بالعربية في الاسفل !!
لمتابعة الفيديوات اللاحقة، اضغط على السهم الاخضر أسفله
نكمل الأسترة و الحلمأة لكي ننتقل بعد ذلك الى التعرف على كيفية التحكم في مجموعة كيميائية.
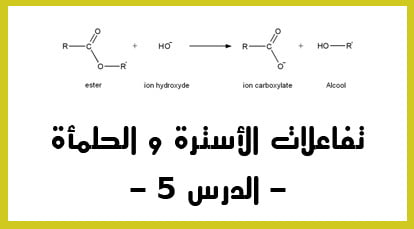
الدقيقة 00:00 : تتمة التعريف بتفاعلات الأسترة و التي تعرف بتفاعل الكحول و حمض كربوكسيلي و أيضا اتمام التعريف بمفهوم المردود r الذي يعرف بكمية المادة الناتجة فعليا من الاستر مقسوما على كمية المادة في حالة التفاعل الأقصى , و هي نفس طريقة حساب تقدم التفاعل To .
الدقيقة 02:55 : ما هي مميزات مردود التفاعل في حالة تفاعلات الأسترة و الحلمأة ؟
- مقدار بدون وحدة.
- و محصور بين 1 و 0 .
- يمكن التعبير عنه بالنسبة المئوية.
الدقيقة 03:38 : كيفية التحكم في سرعة التفاعل ؟
- الرفع من درجة حرارة المتفاعلات – استعمال حمام دافئ – باستخدام هذه الطريقة يأخد التفاعل أقل مدة من الزمن من أجل الوصول الى الحالة النهائية.
- استخدام حفاز catalyseur : و هو عنصر كيميائي يساعد على تسريع التفاعل و لا يكتب في معادلة التفاعل. مثال : اضافة قطرات من حمض الكلوريدريك أو الكبريتيك لانهما يحتويان على أيون +H3O الذي يسرع التفاعل.
الدقيقة 10:50 : كيفية التحكم في الحالة النهائية في حالة تفاعل الأسترة و الحلمأة ؟
أي أننا نريد أن ندفع التفاعل أكثر من الحالة النهائية التلقائية و من أجل القيام بذلك يمكن :
- اضافة أحد المتفاعلات بحيث يكون بوفرة في هذه الحالة يزيح هذا المتفاعل المضاف حالة التوازن في المنحى المباشر.
- حدف أو اخراج أحد النواتج , و يكون مثلا بتجفيف الماء في تفاعل الأسترة.




merci sostade